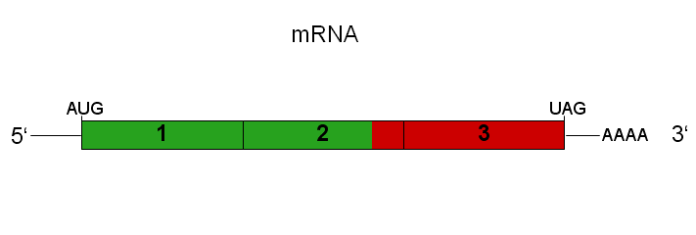
В отличие от обычных мРНК-вакцин, которые кодируют только антигены-мишени, самоамплифицирующиеся мРНК (саРНК) кодируют неструктурные белки, а также промотор, что делает репликоны saРНК способными транскрибироваться in vivo в клетках-хозяевах. Ранние результаты показывают, что их эффективность при введении в меньших дозах не уступает эффективности обычных доз обычной мРНК. Из-за требований к низким дозам, меньшего количества побочных эффектов и большей продолжительности действия saRNA представляется лучшей РНК-платформой для вакцин (в том числе для мРНК вакцин против COVID версии 2.0) и новых терапевтических средств. Ни одна вакцина или лекарство на основе saRNA еще не одобрены для использования человеком. Однако значительный прогресс в этой области может привести к возрождению профилактики и лечения инфекций и дегенеративных заболеваний.
Излишне говорить, что человечество уязвимо перед такими пандемиями, как COVID. Мы все испытали это и так или иначе испытали на себе это влияние; миллионы не смогли дожить до следующего утра. Учитывая, что в Китае тоже была масштабная программа иммунизации против COVID-19, последние сообщения СМИ о вспышках случаев заболевания и смертности в Пекине и его окрестностях вызывают беспокойство. Нельзя недооценивать необходимость готовности и неустанного поиска более эффективных вакцин и терапевтических средств.
Чрезвычайная ситуация, вызванная пандемией COVID-19, дала возможность многообещающей технологии РНК выйти из зрелости. Клинические испытания могут быть завершены в рекордно короткие сроки, и вакцины против COVID на основе мРНК, BNT162b2 (производства Pfizer/BioNTech) и мРНК-1273 (производства Moderna) получили EUA от регулирующих органов и со временем сыграли важную роль в обеспечении защиты от пандемия для людей, особенно в Европе и Северной Америке1. Эти мРНК-вакцины основаны на синтетических РНК-платформах. Это обеспечивает быстрое, масштабируемое и бесклеточное промышленное производство. Но они не лишены ограничений, таких как высокая стоимость, холодовая цепочка поставок, снижение титров антител и многие другие.
Используемые в настоящее время мРНК-вакцины (иногда называемые обычными мРНК-вакцинами или вакцинами 1-го поколения) основаны на кодировании вирусного антигена в синтетической РНК. Невирусная система доставки переносит транскрипт в цитоплазму клетки-хозяина, где экспрессируется вирусный антиген. Затем экспрессированный антиген вызывает иммунный ответ и обеспечивает активный иммунитет. Поскольку РНК легко деградирует и эта мРНК в вакцине не может самотранскрибироваться, в вакцину необходимо вводить значительное количество синтетических транскриптов вирусной РНК (мРНК) для индукции желаемого иммунного ответа. Но что, если в синтетический РНК-транскрипт помимо желаемого вирусного антигена будут включены также неструктурные белки и промоторные гены? Такой РНК-транскрипт будет обладать способностью транскрибироваться или самоамплифицироваться при транспортировке в клетку-хозяин, хотя он будет длиннее и тяжелее, а его транспортировка в клетки-хозяева может быть более сложной.
В отличие от обычной (или неамплифицируемой) мРНК, которая имеет коды только для целевого вирусного антигена, самоамплифицирующаяся мРНК (саРНК) способна транскрибироваться in vivo в клетках-хозяевах благодаря наличию необходимых кодов для неспецифических вирусов. -структурные белки и промотор. Кандидаты на мРНК-вакцины, основанные на самоамплифицирующихся мРНК, называются мРНК-вакцинами второго или следующего поколения. Они предлагают лучшие возможности с точки зрения более низких требований к дозировке, относительно меньшего количества побочных эффектов и большей продолжительности действия/эффектов. (2-5). Обе версии платформы РНК уже давно известны научному сообществу. В ответ на пандемию исследователи выбрали нереплицирующуюся версию платформы мРНК для разработки вакцины ввиду ее простоты и остроты ситуации с пандемией, а также для того, чтобы сначала получить опыт работы с неамплифицирующей версией, как того требовала осторожность. Теперь у нас есть две одобренные мРНК-вакцины против COVID-19, а также несколько кандидатов на вакцины и терапевтические средства, такие как Вакцина против ВИЧ и лечение Болезнь Шарко-Мари-Тута.
saRNA вакцины-кандидаты против COVID-19
Интерес к saRNA-вакцине не нов. Через несколько месяцев после начала пандемии, в середине 2020 г., Маккей и др.. представила кандидатную вакцину на основе saRNA, которая показала высокие титры антител в сыворотке мыши и хорошую нейтрализацию вируса.6. Фаза 1 клинических испытаний VLPCOV-01 (кандидат на самоамплифицирующуюся РНК-вакцину) на 92 здоровых взрослых, результаты которых были опубликованы в препринте в прошлом месяце, пришла к выводу, что введение низких доз этой вакцины-кандидата на основе saRNA индуцирует иммунный ответ, сравнимый с обычной мРНК-вакциной. BNT162b2 и рекомендует ее дальнейшую разработку в качестве бустерной вакцины.7. В другом недавно опубликованном исследовании, проведенном в рамках клинического испытания COVAC1 для разработки стратегии введения бустерной дозы, превосходный иммунный ответ был обнаружен у людей, которые ранее переболели COVID-19 и получили новую самоамплифицирующуюся РНК (саРНК) вакцину против COVID-19 плюс одобренная в Великобритании вакцина8. Доклинические испытания новой пероральной вакцины-кандидата на основе самоамплифицирующейся РНК на мышиной модели выявили высокий титр антител9.
saRNA вакцина-кандидат против гриппа
Используемые в настоящее время противогриппозные вакцины основаны на инактивированных вирусах или синтетических рекомбинантных (синтетический ген НА в сочетании с бакуловирусом).10. Самоамплифицирующаяся вакцина-кандидат на основе мРНК может индуцировать иммунитет против нескольких вирусных антигенов. Доклинические испытания бицистронной вакцины A/H5N1 с sa-мРНК-кандидатом против гриппа на мышах и хорьках выявили сильнодействующие антитела и Т-клеточный ответ, требующие оценки на людях в клинических испытаниях11.
Вакцинам против COVID-19 уделяется пристальное внимание по очевидным причинам. Некоторые доклинические работы по применению РНК-платформ были проведены для других инфекций и неинфекционных заболеваний, таких как рак, болезнь Альцгеймера и наследственные заболевания; однако ни одна вакцина или лекарство на основе saRNA еще не одобрены для использования человеком. Необходимо провести дополнительные исследования по использованию вакцин на основе saRNA, чтобы всесторонне понять их безопасность и эффективность для использования на людях.
Ссылки:
- Прасад У., 2020 г. мРНК-вакцина против COVID-19: веха в науке и переломный момент в медицине. Научный европеец. Опубликовано 29 декабря 2020 г. Доступно в Интернете по адресу http://scientificeuropean.co.uk/medicine/covid-19-mrna-vaccine-a-milestone-in-science-and-a-game-changer-in-medicine/
- Блум К., ван ден Берг Ф. и Арбутнот П. Самоамплифицирующиеся РНК-вакцины от инфекционных заболеваний. Джин Тер 28. С. 117–129 (2021). https://doi.org/10.1038/s41434-020-00204-y
- Пурсеф ММ и др. 2022. Самоамплифицирующиеся мРНК-вакцины: механизм действия, дизайн, разработка и оптимизация. Открытие наркотиков сегодня. Том 27, выпуск 11, ноябрь 2022 г., 103341. DOI: https://doi.org/10.1016/j.drudis.2022.103341
- Блэкни АК и др. 2021. Обновленная информация о разработке самоамплифицирующейся мРНК-вакцины. Вакцины 2021, 9(2), 97; https://doi.org/10.3390/vaccines9020097
- Анна Блэкни; Новое поколение РНК-вакцин: самоамплифицирующаяся РНК. Biochem (Лондон), 13 августа 2021 г.; 43 (4): 14–17. дои: https://doi.org/10.1042/bio_2021_142
- McKay, PF, Hu, K., Blakney, AK et al. Самоамплифицирующаяся РНК-кандидат липидных наночастиц SARS-CoV-2 вызывает высокие титры нейтрализующих антител у мышей. Нац коммуна 11, 3523 (2020). https://doi.org/10.1038/s41467-020-17409-9
- Акахата В. и др. 2022. Безопасность и иммуногенность самоамплифицирующейся РНК-вакцины против SARS-CoV-2, экспрессирующей закрепленный RBD: рандомизированное слепое исследование фазы 1. Препринт medRxiv 2022.11.21.22281000; Опубликовано 22 ноября 2022 г. doi: https://doi.org/10.1101/2022.11.21.22281000
- Эллиотт Т. и др. (2022)Усиленные иммунные реакции после гетерологичной вакцинации самоамплифицирующимися РНК и мРНК вакцинами против COVID-19. PLoS Pathog 18(10): e1010885. Опубликовано: 4 октября 2022 г. DOI: https://doi.org/10.1371/journal.ppat.1010885
- Кейха Р., Хашеми-Шахри С.М. и Джебали А. Оценка новых пероральных вакцин на основе самоамплифицирующихся липидных наночастиц РНК (саРНК ЛНЧ), ЛНЧ Lactobacillus plantarum, трансфицированных saRNA, и Lactobacillus plantarum, трансфицированных saRNA, для нейтрализации SARS-CoV -2 варианта альфа и дельта. Научный представитель 11, 21308 (2021). Опубликовано: 29 октября 2021 г. https://doi.org/10.1038/s41598-021-00830-5
- CDC 2022. Как производятся вакцины против гриппа. Доступно онлайн по адресу https://www.cdc.gov/flu/prevent/how-fluvaccine-made.htm Доступ к 18 Декабрь 2022.
- Chang C., et al 2022. Самоамплифицирующиеся мРНК бицистронные вакцины против гриппа вызывают перекрестные иммунные реакции у мышей и предотвращают инфекцию у хорьков. Методы молекулярной терапии и клиническая разработка. Том 27, 8 декабря 2022 г., страницы 195–205. https://doi.org/10.1016/j.omtm.2022.09.013